Revisão
|
|
| Cannabis sativa L.: Uma revisão crítica sobre canabinoides, legislação e métodos analíticos Cannabis sativa L.: A critical review of cannabinoids, legislation, and analytical methods |
|
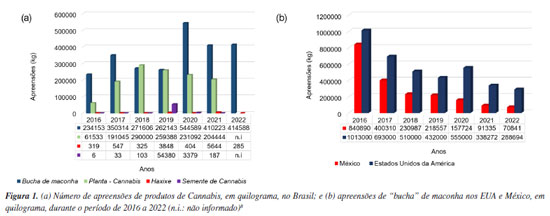
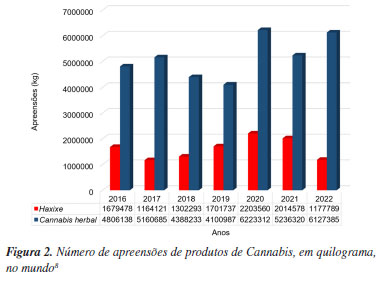
João Victor M. de AlmeidaI,II; Eclair Venturini FilhoIII; Nathália S. ConceiçãoI,II; Alan R. PereiraI,II; Julie M. M. FigueiredoIII; Ricardo M. KusterI; Hildegardo S. FrançaIII; Nayara A. dos SantosI,II,III; Wanderson RomãoI,II,III* I Departamento de Química, Universidade Federal do Espírito Santo, 29075-910 Vitória - ES, Brasil Recebido: 07/08/2025; *e-mail: wandersonromao@gmail.com Editor responsável pelo artigo: Jorge M. David Forensic chemistry plays a crucial role in criminal investigations, utilizing techniques to analyze evidence such as gunshot residues, explosives, and illicit drugs. Among these, Cannabis is widely studied due to its medical and recreational use, especially considering that it is the most trafficked drug worldwide. The plant contains over 700 compounds, including around 120 cannabinoids. Overall, cannabinoids have been used to treat several health problems such as chronic pain, nausea, and vomiting, among others. Despite its therapeutic potential, recreational use is associated with health risks, including cardiovascular issues, cognitive impairment, mental disorders, and addiction. The cannabinoids market has increased significantly along with interest in Cannabis products as a drug, leading to a need for novelty in instrumental analysis and methods to support quality control laboratories and scientific police forces. In this sense, the analysis of cannabinoids in various matrices primarily relies on chromatographic techniques. Gas chromatography (GC), often coupled with mass spectrometry (MS) or a flame ionization detector (FID), is widely used. However, liquid chromatography (LC) offers advantages in preserving acidic cannabinoids and preventing their degradation. Therefore, all the processes concerning Cannabis were addressed in this study, from its composition to legislation and chemical evaluation. INTRODUÇÃO A aplicação de procedimentos e técnicas analíticas na investigação criminal é de extrema importância na resolução de crimes, no apuramento de fatos e no levantamento de dados para a sustentação da ação criminal.1 Dentre os ramos das ciências forenses, a química forense, que teve seu início no final do século XVII, tem alta relevância e se baseia na aplicação de conhecimentos da química para a produção de provas materiais em prol da justiça.1 Suas aplicações incluem análise de resíduos de disparo, investigação de incêndios e explosivos, detecção de venenos, identificação de drogas e revelação de vestígios biológicos.2-4 Particularmente na análise de drogas, fármacos e substâncias psicoativas, diferentes técnicas possibilitam a identificação e quantificação dos princípios ativos analisados.3 Em geral, o uso dessas drogas tem como principais finalidades a busca pelos efeitos medicinais e/ou psicotrópicos, que interferem no sistema nervoso central (SNC). O uso dessas substâncias, lícitas ou ilícitas, está associado a impactos físicos, psicológicos e sociais.3,5 Uma das categorizações das drogas relaciona-se com sua ação principal no SNC, que pode ser: (i) depressora do SNC como o álcool, e opioides como heroína e morfina; (ii) estimulante do SNC, como as anfetaminas e cocaína; e (iii) perturbadora, como o LSD, e Δ9-tetraidrocanabinol (Δ9-THC).3,6,7 Dentre as drogas de abuso ilícitas, a maconha, produto da planta Cannabis, é mundialmente a mais utilizada, atingindo cerca de 2,5% da população mundial em 2018.6 Além da maconha, outros produtos comuns da Cannabis são o haxixe e o óleo de haxixe. Em relação aos efeitos dessa droga no usuário, em geral, se baseiam em distorções sensoriais e alterações na percepção da realidade.3,7 Devido o constante aumento no número de usuários, é possível observar um aumento do tráfico de drogas e suas apreensões.6 Dados da United Nations Office on Drugs and Crime (UNODC),8 indicam que, entre 2016 e 2022, apreensões de maconha em forma de "buchas" cresceram 77%, enquanto outras formas da planta apresentaram queda no mesmo período (Figura 1). Apreensões de buchas de maconha são significativas no Brasil e em outros países da América, como os Estados Unidos da América (EUA) e México, porém é possível observar a diminuição do mesmo entre os anos de 2016 e 2022, com queda de 71% nos EUA e de 91% no México.8 Em 2021, a Suprema Corte do México descriminalizou o uso recreativo privado de Cannabis por adultos, o que pôde ter influenciado o número de apreensões.9 Nos EUA, o cânhamo foi retirado da definição de maconha em 2018, fazendo com que o canabidiol (CBD) não seja considerado uma substância controlada. Em contrapartida, o uso de maconha no país não é permitido sob lei federal, e pode gerar penalidades para usuários. No entanto, é comum que estados do país tenham leis que permitem o uso medicinal e recreativo da maconha. Nesse sentido, 38 estados, Washington DC, Porto Rico, Guam e Ilhas Virgens Americanas permitem o uso medicinal de maconha, enquanto que 24 estados, Washington DC, Guam e as Ilhas Marianas Setentrionais aprovaram leis que permitem o uso recreativo da maconha.10 No aspecto global, as apreensões de produtos de haxixe declinaram em 2022 e os de Cannabis herbal aumentaram entre 2021 e 2022 (Figura 2).8
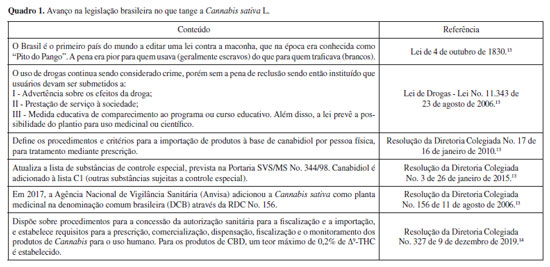
No Brasil, a Lei No. 11.343 de 2006,5 instituiu o Sistema Nacional de Políticas Públicas sobre Drogas, que trata de diversos assuntos relacionados ao uso de drogas e seu tráfico, e define os crimes relacionados. Nesse sentido, a Lei classifica como drogas, substâncias ou produtos capazes de causar dependência, especificados ou relacionados em listas atualizadas periodicamente pelo Poder Executivo da União. Além disso, conforme o Art. 2º,5 em todo o território nacional, são proibidos, o plantio, a cultura, a colheita e a extração de compostos a partir de substratos vegetais com objetivo de produzir drogas, com algumas exceções regidas na lei. Como penalidade, a exportação, importação, a produção, e o fornecimento de droga, mesmo de forma gratuita, acarretam ao infrator à reclusão de 5 a 15 anos com o pagamento de R$ 500,00 a 1500,00 dias-multa.5 No entanto, sobre o uso medicinal de produtos medicinais contendo canabinoides, a Resolução da Diretoria Colegiada No. 327 de 2019,11 regulamenta a comercialização desses produtos, permitindo a venda, sob prescrição médica e com retenção de receita de canabidiol (CBD) e Δ9-THC, e indicando-os para prescrição somente se outras opções de tratamento existentes não obtiveram o resultado esperado. Ademais, o uso desses canabinoides é regulamentado para tratamento de problemas de saúde específicos, com indicação do uso de Δ9-THC acima de 0,2% em condições clínicas irreversíveis ou em cuidados paliativos.11 No caso de uso medicinal pessoal, a Resolução da Diretoria Colegiada No. 355 de 2020,12 estabelece critérios e procedimentos para importação de produtos de Cannabis por pessoas físicas. Em síntese, a legislação relacionada à Cannabis apresenta histórico extenso e tem evoluído progressivamente ao longo dos anos (Quadro 1).
No aspecto global, os usos medicinais e recreativos da Cannabis sativa são permitidos em alguns países, enquanto para outros, é permitido apenas o seu uso medicinal. Dentro desse contexto, Canadá, Uruguai, e Austrália permitem o uso recreativo da planta, mesmo que em alguns casos, a venda não tenha sido regulamentada ainda. Por outro lado, o continente europeu possui o maior mercado de Cannabis do mundo, sendo que 23 países já legalizaram o seu uso medicinal e recreativo.15 Diante desse panorama, este trabalho apresenta uma revisão crítica sobre a Cannabis, abrangendo histórico, legislação e avanços nas técnicas de análise química. Foram consultadas bases de dados como PubMed Central, Web of Science, Scopus e Chemical Abstracts, além de legislações e literatura especializada. Cannabis A Cannabis, gênero de origem asiática, apresenta registros de cultivo na Ásia Central desde cerca de 12.000 a.C., inicialmente para obtenção de fibras e tecidos.16 Seu uso expandiu-se ao longo dos séculos para fins medicinais, religiosos e recreativos, sendo classificada botanicamente em 1753.16-18 Atualmente, reconhece-se a espécie Cannabis sativa L., subdividida em C. sativa, C. indica e C. ruderalis, além de híbridos e distintos quimiotipos.19 Dentre as subespécies, a C. sativa possui maior teor de Δ9-THC em relação ao CBD e o perfil de terpenos atribui um cheiro mais "herbal" ou "doce", enquanto a C. indica produz mais CBD do que a C. sativa e os terpenos atribuem um cheiro mais "azedo". Ademais, a C. ruderalis possui um teor de CBD e Δ9-THC mais próximo um do outro, e costuma ser uma planta do tipo selvagem, que cresce espontaneamente na natureza.19 Do ponto de vista químico, já foram descritas mais de 700 substâncias na Cannabis, incluindo mais de 120 canabinoides, distribuídos em 11 classes: Δ9-THC, canabigerol (CBG), canabicromeno (CBC), canabidiol (CBD), Δ8-tetraidrocanabinol (Δ8-THC), canabinol (CBN), canabiciclol (CBL), canabielsoin (CBE), canabinodiol (CBND), canabitriol (CBT) e canabinoides diversos.20-22 Esses canabinoides ocorrem principalmente em formas ácidas, como Δ9-THCA e CBDA, que por descarboxilação térmica originam os canabinoides neutros correspondentes (Figura 3).23,24
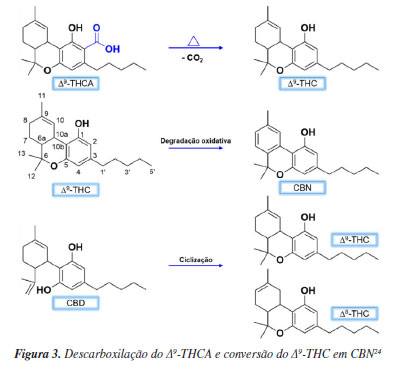
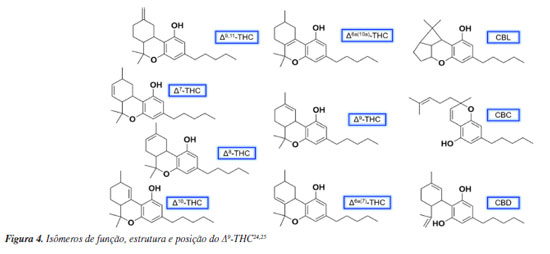
Δ9-THC e seus isômeros O Δ9-THC (C21H30O2), massa molecular (MM) = 314,469 g mol−1, pKa = 10,6, (+)-(6aR,10aR)-6,6,9-trimethyl-3-pentyl-6a,7,8,10a-tetrahydro-6H-benzo[c]chromen-1-o, é o principal composto psicoativo, encontrado em maior concentração nas flores pistiladas (10-12%), seguido por folhas (1-2%), caule (0,1-0,3%) e raízes (< 0,03%).24 Além de ocorrer naturalmente, pode ser obtido por descarboxilação do Δ9-THCA ou por ciclização do CBD, processo também observado na planta.24 A concentração de Δ9-THC, contudo, decresce ao longo do tempo, devido à conversão em CBN.24 O Δ9-THC possui 4 estereoisômeros: (-)-Δ9-trans-THC, (+)-Δ9-trans-THC, (-)-Δ9-cis-THC e (+)-Δ9-cis-THC. Dentre esses, o (-)-Δ9-trans-THC é o que está presente de forma mais abundante na planta e é o principal composto com propriedades psicoativas da Cannabis. Quando se trata da composição e quantidade de diferentes canabinoides presentes na planta, os canabinoides Δ9-THC, CBD e CBC são os principais constituintes, sendo que 95% deles podem ser encontrados na sua forma ácida em amostra de biomassa.24 Ademais, o Δ9-THC possui cinco isômeros principais, sendo eles Δ8-trans-THC, CBL, CBD, CBC e CBD (Figura 4).24,25
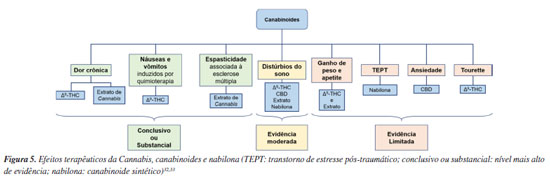
APLICAÇÕES TERAPÊUTICAS Uso recreativo e riscos O consumo recreativo de Cannabis está associado a uma série de efeitos adversos. Relatos incluem problemas cardiovasculares em jovens saudáveis, além de ansiedade, paranoia, disforia, comprometimento cognitivo e complicações gestacionais, como baixo peso ao nascer.26 O uso crônico tem sido relacionado a alterações estruturais e funcionais do cérebro, aumento do risco de acidente vascular cerebral, câncer respiratório e de testículo, além de anedonia e dependência.26 Estudos epidemiológicos também apontam associação com sintomas psicóticos e esquizofrenia, especialmente entre usuários frequentes.26-28 Aproximadamente 10% dos consumidores desenvolvem dependência, e casos de síndrome de hiperêmese por canabinoides vêm sendo descritos.27,28 Há ainda riscos relacionados ao fumo passivo: evidências preliminares indicam a presença de metabólitos de Δ9-THC em pessoas expostas à fumaça de segunda mão.29 Potencial terapêutico Apesar dos riscos, estudos recentes apontam benefícios terapêuticos do uso controlado de canabinoides. O CBD, isolado ou em combinação com Δ9-THC, tem sido empregado no manejo de epilepsia, dor crônica, ansiedade, depressão, esclerose múltipla e insônia (Figura 5).30-33 No entanto, a eficácia de muitas dessas aplicações ainda carece de confirmação robusta: grande parte dos ensaios clínicos é composta por amostras reduzidas e de curta duração, o que limita a avaliação de efeitos a longo prazo.34-36
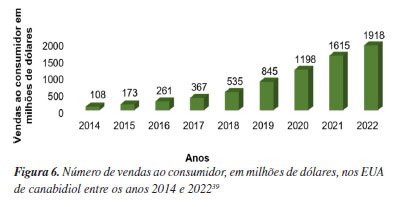
Questões como tolerância, dependência e interações medicamentosas permanecem insuficientemente esclarecidas. Há relatos de uso em crianças com transtorno de déficit de atenção e outros distúrbios de neurodesenvolvimento, embora faltem evidências conclusivas sobre a segurança.31,34-37 Mercado e regulamentação Nos Estados Unidos, onde o cânhamo foi legalizado em 2018, o mercado de CBD apresenta rápido crescimento: projeções indicam faturamento global próximo de 105 bilhões de dólares até 2026.30‑35,38 Segundo a Statista,39 entre 2022 e 2024 houve um aumento de 1.810 bilhões de dólares obtidos na venda de produtos de CBD (Figura 6). No Brasil, a Anvisa reportou a venda de 13 milhões de produtos derivados de Cannabis para uso medicinal em 2021.30,31,34,35,38 Estimativas de 2023 apontam 430 mil pacientes em tratamento, sendo a maioria por importação, seguida por farmácias e associações.40
Esse cenário evidencia a necessidade de maior rigor no controle de qualidade. A literatura41-43 aponta a ocorrência de adulterações, com presença de canabinoides sintéticos ou concentrações de Δ9-THC acima dos limites legais. Análises de produtos europeus, por exemplo, já identificaram teores de Δ9-THC superiores ao limite estabelecido pela European Food Safety Authority (EFSA).44,45 No Brasil, empresas devem comprovar qualidade e segurança para obter autorização sanitária. A ausência de métodos compendiais específicos para canabinoides, entretanto, representa um desafio regulatório.11,22,46 Atualmente, produtos comercializados por laboratórios como NuNature, Farmanguinhos e Mantecorp apresentam concentrações de CBD variando entre 17 e 160 mg mL-1, havendo inclusive aprovações para formulações com teor de Δ9-THC acima de 0,2% em condições clínicas irreversíveis.47 Associações sem fins lucrativos também têm se destacado na oferta de produtos, com concentrações entre 125 e 6.000 mg e ampla variação de preços.40 Em 2024, a Anvisa48 ampliou a regulamentação, permitindo a prescrição veterinária de produtos à base de Cannabis sativa L. mediante autorização do Ministério da Agricultura e Pecuária (MAPA).
EXTRAÇÃO DE CANABINOIDES O preparo adequado da amostra é determinante para o rendimento da extração de canabinoides. A Cannabis contém cerca de 80% de água; por isso, a secagem é etapa necessária não apenas para a recuperação dos compostos, mas também para evitar a proliferação microbiana e a perda de qualidade do material.49 Métodos como secagem ao ar, em estufa, por congelamento ou curamento são empregados, e variam quanto ao impacto na estabilidade e no teor final de canabinoides.49 Quanto à extração, diferentes estratégias têm sido utilizadas para aumentar a recuperação dos compostos em matrizes vegetais ou oleosas. Entre os métodos clássicos, destacam-se a maceração e a extração Soxhlet, enquanto técnicas mais recentes incluem extração líquido-pressurizada, assistida por micro-ondas, ultrassom, fluido supercrítico e microextração em fase sólida.50,51 Dentre essas, a sonicação vem recebendo maior atenção pela eficiência, menor tempo de preparo e economia de solventes.50 A escolha do solvente é fator crítico. Solventes orgânicos permanecem os mais empregados.50,52 De acordo com a UNODC,24 solventes apolares, como hexano e éter de petróleo, favorecem a extração de canabinoides neutros; para os ácidos, são preferíveis solventes polares, como etanol, metanol e isopropanol, embora estes extraiam também as formas neutras. Assim, a definição do solvente deve considerar o perfil de compostos de interesse e o objetivo analítico.
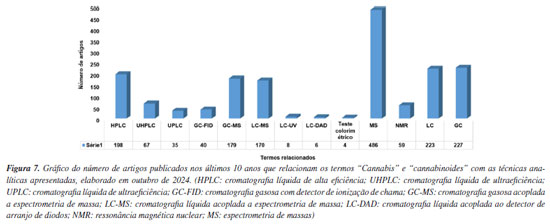
ANÁLISE DE CANABINOIDES A quantificação de canabinoides em diferentes matrizes é realizada principalmente por cromatografia líquida (LC) e cromatografia a gás (GC), associadas ao analisador espectrometria de massas (MS) ou detectores de técnicas espectofotométricas ou ionização em chama (FID).53,54 Dentre as técnicas cromatograficas, a LC apresenta vantagem na análise de canabinoides ácidos, pois evita a descarboxilação observada na GC devido às altas temperaturas.54 Uma análise bibliométrica realizada a partir do Web of Science, com os termos "Cannabis" e "cannabinoids" associados a técnicas analíticas, mostra a predominância de LC-MS e GC-MS na última década (Figura 7). Esse resultado reflete a elevada sensibilidade da MS e a importância das etapas cromatográficas para a separação de isômeros, especialmente relevantes para aplicações em química medicinal.
Além da cromatografia, métodos preliminares como testes colorimétricos ainda encontram aplicação, enquanto a ressonância magnética tem surgido como alternativa exploratória, embora com uso restrito para quantificação.6,44,55-59 A análise da nuvem de palavras construída com os 50 termos mais citados em Author's Keywords (Figura 8) reforça o protagonismo de LC-MS, LC-MS/MS e GC-MS.

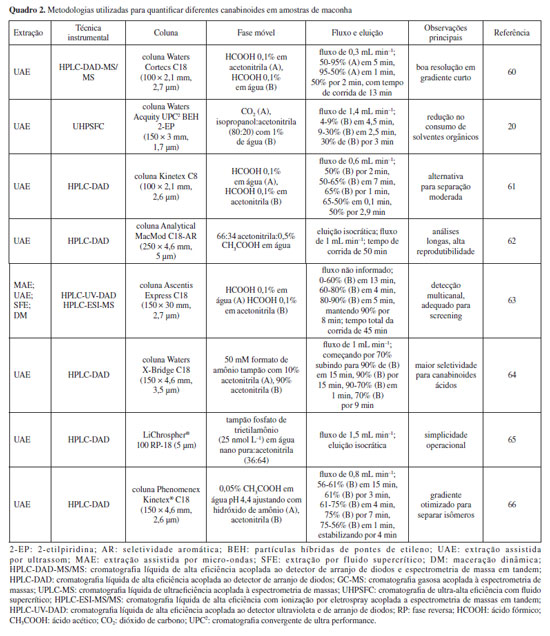
Nesse sentido, considerando as principais técnicas utilizadas, uma revisão de metodologias desenvolvidas com LC foi realizada, a fim de detalhar o processo de análise de maconha (Quadro 2).
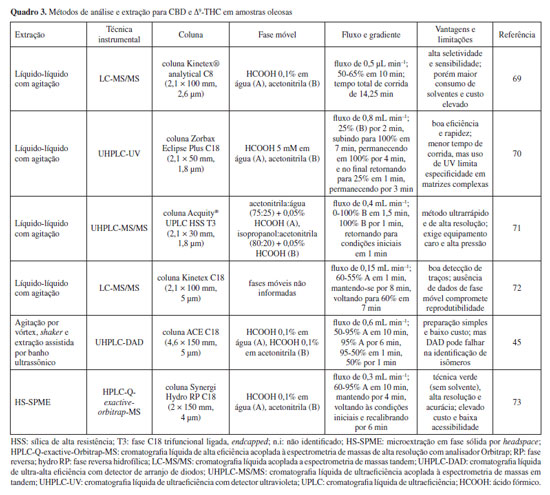
Apesar do avanço de tecnologias como cromatografia líquida de ultraeficiência (UPLC) e cromatografia líquida de ultraeficiência (UHPLC), a cromatografia líquida de alta eficiência (HPLC) permanece como a técnica mais empregada para a análise de canabinoides.20,24,61-67 Essa predominância se deve, em parte, à maior disponibilidade instrumental e à robustez metodológica, embora esteja associada ao consumo elevado de solventes (fluxos acima de 1 mL min-1) e consequente maior geração de resíduos. A UHPLC, por sua vez, apresenta vantagens como maior resolução e menor tempo de análise, mas exige operação em pressões elevadas e otimização cuidadosa do gradiente, da temperatura e do volume de solvente.67,68 A complexidade da matriz de Cannabis impõe a necessidade de separar adequadamente canabinoides estruturalmente similares, sobretudo isômeros. A escolha da fase móvel e do gradiente de eluição influencia diretamente a resolução obtida. Trabalhos recentes45,69 indicam o uso predominante de soluções de ácido fórmico (0,1%) ou ácido acético em água como fase aquosa, combinadas com acetonitrila acidificada como fase orgânica. Tempos de corrida variam amplamente (de menos de 10 até mais de 40 min), sendo ajustados conforme o conjunto de analitos-alvo.67 Em relação às colunas, observa-se a predominância de C18, atribuída à sua maior capacidade de interação hidrofóbica e consequente aumento da resolução cromatográfica. Essa característica favorece a separação de isômeros, cujo fracionamento é particularmente desafiador. Recentemente, colunas C8 também têm sido utilizadas, demonstrando potencial para maior seletividade em gradientes otimizados.65 Ainda assim, há espaço para exploração de colunas alternativas, como C30 e hilic, que podem ampliar a seletividade em metodologias pouco exploradas. No preparo de amostras, destaca-se o uso de extração assistida por ultrassom (UAE), frequentemente associada à HPLC. Essa técnica tem se mostrado eficiente ao reduzir tempo de extração e consumo de solventes, além de aumentar o rendimento em comparação com métodos tradicionais como maceração, extração assistida por micro-ondas e extração com fluido supercrítico.20,24,60-67 No entanto, para estudos cujo objetivo é o fracionamento completo dos constituintes da planta, a maceração continua sendo indicada. Apesar da variedade de abordagens cromatográficas descritas na literatura para a análise de canabinoides em matrizes oleosas, observa-se que o número de métodos validados permanece reduzido. Além disso, grande parte dos protocolos disponíveis encontra-se depositada sob a forma de patentes, desenvolvidos pelos próprios fabricantes, o que limita o acesso a metodologias independentes e comparáveis.44,45 Considerando a relevância do tema, apresenta-se no Quadro 3 um panorama de metodologias recentes baseadas em LC para a análise de amostras oleosas contendo CBD e Δ9-THC.
Em geral, o processo cromatográfico aplicado a óleos segue princípios semelhantes àqueles empregados para amostras vegetais (Quadros 2 e 3). A principal diferença reside no preparo da amostra: óleos podem ser diluídos, o que possibilita métodos mais rápidos e práticos em comparação às matrizes vegetais, frequentemente complexas e ricas em interferentes. Essa diluição é usualmente promovida por agitação, vortexação ou sonicação, reduzindo tempo de preparo e consumo de solventes.45,69-73 No entanto, a literatura revela algumas limitações. Primeiramente, grande parte dos trabalhos recorre a amostras enriquecidas em laboratório, sem avaliar produtos comercialmente disponíveis. Essa escolha pode negligenciar variáveis críticas, como a presença de contaminantes, adulterantes ou excipientes diversos, que influenciam diretamente a seletividade e a robustez dos métodos analíticos. Em segundo lugar, embora se observem esforços na otimização do tempo de corrida cromatográfica, a ausência de padronização entre gradientes e fases móveis dificulta a comparação direta entre resultados. Do ponto de vista da sustentabilidade analítica, a escolha da técnica é um fator crucial. Métodos baseados em UHPLC tendem a consumir menores volumes de solventes e gerar menos resíduos quando comparados ao HPLC convencional. Nesse contexto, técnicas emergentes como a microextração em fase sólida por headspace (HS‑SPME) associada a espectrometria de massas de alta resolução apresentam vantagens por dispensarem grandes volumes de solventes orgânicos, reduzindo o impacto ambiental. No âmbito regulatório, observa-se carência de metodologias harmonizadas que atendam simultaneamente às exigências de agências como Anvisa, EFSA e Food and Drug Administration (FDA). Tal lacuna compromete tanto a comparabilidade internacional quanto a confiabilidade na avaliação de produtos comerciais. Dessa forma, torna-se urgente o desenvolvimento de protocolos validados que considerem não apenas a eficiência analítica, mas também a sustentabilidade e a conformidade regulatória. Assim, persiste uma lacuna metodológica importante: a validação de métodos quantitativos de canabinoides em óleos comerciais que contemplem a diversidade de excipientes empregados. O desenvolvimento e a validação dessas metodologias são essenciais para garantir qualidade, segurança, reprodutibilidade e alinhamento com diretrizes regulatórias internacionais.
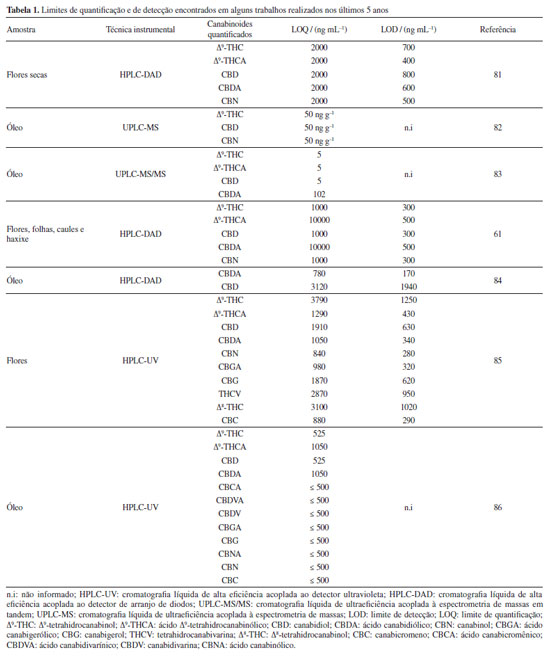
VALIDAÇÃO ANALÍTICA A validação de métodos analíticos é etapa essencial no desenvolvimento de metodologias, pois permite comprovar a qualidade e a adequação do método para o propósito a que se destina. No Brasil, a Resolução da Diretoria Colegiada (RDC) No. 166 de 2017,74 da Anvisa e o DOQ-CGCRE-008,75 do Inmetro definem critérios e procedimentos de validação, harmonizados com documentos internacionais.76,77 Segundo o DOQ-CGCRE-008,75 as figuras de mérito incluem seletividade, linearidade (faixa de trabalho e faixa linear), sensibilidade, limites de detecção (LOD) e quantificação (LOQ), exatidão (tendência/recuperação), precisão e robustez. Para métodos quantitativos, todos os parâmetros, exceto a robustez, são obrigatórios; já em métodos qualitativos, apenas seletividade e LOD são requeridos.74-80 Nos últimos cinco anos, diversos trabalhos reportaram a validação ou verificação de métodos para a quantificação de canabinoides em diferentes matrizes. A Tabela 1 sintetiza valores de LOD e LOQ obtidos em estudos recentes,81-86 permitindo comparar a sensibilidade de distintas técnicas cromatográficas e detectores.
De maneira geral, observa-se que métodos baseados em LC acoplada à espectrometria de massas (LC-MS/MS e UPLC-MS) apresentam limites de detecção e quantificação até três ordens de magnitude inferiores aos obtidos por técnicas espectrofotométricas (HPLC-DAD e HPLC-UV), confirmando sua superioridade para análise de canabinoides em matrizes complexas. Contudo, chama a atenção a falta de reporte completo de todas as figuras de mérito, especialmente robustez e recuperação, em parte significativa dos trabalhos. Esse cenário evidencia a necessidade de padronização e validação mais abrangente dos métodos aplicados a produtos derivados de Cannabis, sobretudo diante de sua crescente utilização em contextos clínicos e regulatórios.
CONCLUSÕES A análise de canabinoides tem se mostrado estratégica tanto no contexto científico quanto no mercado e no combate ao tráfico de drogas. A literatura evidencia avanços em técnicas cromatográficas, sobretudo LC-MS, mas também revela limitações: poucos métodos validados, predominância de protocolos patenteados e escassez de estudos aplicados a produtos comerciais. Diante disso, torna-se essencial o desenvolvimento de metodologias reprodutíveis, sensíveis e devidamente validadas, capazes de assegurar resultados comparáveis entre diferentes laboratórios. A validação rigorosa, seguindo diretrizes nacionais e internacionais, deve ser priorizada para garantir confiabilidade às análises de Cannabis, fortalecendo sua aplicação tanto no Brasil quanto no cenário internacional.
DECLARAÇÃO DE DISPONIBILIDADE DE DADOS Os autores afirmam que todos os dados estão disponíveis no texto.
AGRADECIMENTOS Os autores agradecem à Fundação de Amparo à Pesquisa e Inovação do Espírito Santo (FAPES) No. 03/2021 - Universal (492/2021); No. 15/2022 - PROFIX 2022 (714/2022 P: 2022-SS849); No. 019/2022 - Núcleos Capixabas de Excelência em Pesquisa (991/2022 P; 2022-5KMF0); edital FAPES No. 21/2022 - Apoio à Infraestrutura de Pesquisa (1069/2022 P: 2022-98VRN); e ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq, 310057/2020-5, INCT Forense) pelo apoio financeiro. Este estudo também foi financiado em parte pela Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES, código de financiamento 1).
CONTRIBUIÇÕES DO AUTOR João V. M. de Almeida foi responsável por conceituação, curadoria de dados, análise formal, investigação, visualização, redação (rascunho original, revisão e edição); Eclair V. Filho por redação (revisão e edição); Nathália S. Conceição por redação (revisão e edição); Alan R. Pereira por redação (revisão e edição); Julie M. M. Figueiredo por visualização; Ricardo M. Kuster por redação (revisão e edição); Hildegardo S. França por redação (revisão e edição); Nayara A. dos Santos por visualização, administração de projetos, análise formal; Wanderson Romão por visualização, administração de projetos, redação (revisão e edição), análise formal.
REFERÊNCIAS 1. Oliveira Junior, A.; Importância das Atividades de Investigação e Inteligência Policial para o Sistema de Justiça Criminal e seu Aprimoramento no Brasil, 2012. [Link] acessado em setembro 2025 2. Santos, F. R. D.: A Química Forense como Tema Contextualizador no Ensino de Química; Dissertação de Mestrado, Universidade Cruzeiro do Sul, Cruzeiro do Sul, Brasil, 2020. [Link] acessado em setembro 2025 3. Silva, M.: Contributo da Química Forense na Detecção de Drogas de Abuso; Dissertação de Mestrado, Universidade de Lisboa, Lisboa, Portugal, 2013. [Link] acessado em setembro 2025 4. Romão, W.; Schwab, N. V.; Izabel, M.; Bueno, M. S.; Sparrapan, R.; Eberlin, M. N.; Martiny, A.; Sabino, B. D.; Quim. Nova 2011, 34, 10. [Crossref] 5. Presidência da República Casa Civil; Lei No. 11.343, de 23 de agosto de 2006, Institui o Sistema Nacional de Políticas Públicas sobre Drogas - Sisnad; Prescreve Medidas para Prevenção do Uso Indevido, Atenção e Reinserção Social de Usuários e Dependentes de Drogas; Estabelece Normas para Repressão à Produção Não Autorizada e ao Tráfico Ilícito de Drogas; Define Crimes e dá Outras Providências; Diário Oficial da União (DOU), Brasília, Brasil, 2006. [Link] acessado em setembro 2025 6. Bordin, D. C.; Messias, M.; Lanaro, R.; Cazenave, S. O. S.; Costa, J. L.; Quim. Nova 2012, 35, 10. [Crossref] 7. Santos, N. A. D.: Análises de Padrões Isoméricos de Canabinoides e Produtos de Cannabis por GC-MS, GCxGC-qMS e UPLC Acoplado a Espectrometria de Massas de Mobilidade Iônica (TWIM-MS); Dissertação de Mestrado, Universidade Federal do Espírito Santo, Vitória, Brasil, 2018. [Link] acessado em setembro 2025 8. United Nations Office on Drugs and Crime (UNODC), https://www.unodc.org/unodc/en/data-and-analysis/Previous-reports.html, acessado em setembro 2025. 9. BBC News, Maconha: México é 2º País da América Latina a Descriminalizar Uso Recreativo da Droga, https://surl.li/umwukt, acessado em setembro 2025. 10. Congress.gov, https://www.congress.gov/crs-product/IF12270, acessado em setembro 2025. 11. Agência Nacional de Vigilância Sanitária (Anvisa); Resolução da Diretoria Colegiada (RDC) No. 327, de 09 de dezembro de 2019, Dispõe sobre os Procedimentos para a Concessão da Autorização Sanitária para a Fabricação e a Importação, bem como Estabelece Requisitos para a Comercialização, Prescrição, a Dispensação, o Monitoramento e a Fiscalização de Produtos de Cannabis para Fins Medicinais, e dá Outras Providências; Diário Oficial da União (DOU), Brasília, No. 239, de 11/12/2019, p. 194. [Link] acessado em setembro 2025 12. Agência Nacional de Vigilância Sanitária (Anvisa); Resolução da Diretoria Colegiada No. 355, de 23 de março de 2020, Dispõe sobre a Suspensão dos Prazos Processuais Afetos aos Requerimentos de Atos Públicos de Liberação de Responsabilidade da Anvisa em Virtude da Emergência de Saúde Pública Internacional Relacionada ao SARS-CoV-2; Diário Oficial da União (DOU), Brasília, Brasil, 2020. [Link] acessado em setembro 2025 13. Martins, D. A.; Posso, I. P.; Brazilian Journal of Pain 2023, 6, 2. [Crossref] 14. Supremo Tribunal Federal, STF Define 40 gramas de Maconha como Critério para Diferenciar Usuário de Traficante, https://surl.li/wjbgzb, acessado em setembro 2025. 15. Veja, Os mais de 40 Países onde se Pode Fumar Maconha, https://veja.abril.com.br/mundo/os-mais-de-40-paises-onde-se-pode-fumar-maconha, acessado em setembro 2025. 16. Leghissa, A.; Hildenbrand, Z. L.; Schug, K. A.; J. Sep. Sci. 2018, 41, 398. [Crossref] 17. Honório, K. M.; Arroio, A.; Silva, A. B. F. S.; Quim. Nova 2006, 29, 2. [Crossref] 18. United States Department of Agriculture, https://plants.usda.gov/classification/70749, acessado em setembro 2025. 19. Macpartland, J. M.; Cannabis Cannabinoid Res. 2018, 3, 1. [Crossref] 20. Wang, M.; Wang, Y. H.; Avula, B.; Radwan, M. M.; Wanas, A. S.; Mehmedic, Z.; Van Antwerp, J.; Elsohly, M. A.; Khan, I. A.; J. Forensic Sci. 2017, 62, 3. [Crossref] 21. Nascimento, I. R.; Costa, H. B.; Souza, L. M.; Soprani, L. C.; Merlo, B. B.; Romão, W.; Anal. Methods2015, 7, 4. [Crossref] 22. Dantas, A. S. C.; Souza, M. N.; Lima, P. C.; Santana, D. S.; Maranho, R. L. N.; Colonese, A.; Ochs, S. M.; Monteiro, M. A.; Quim. Nova 2023, 46, 3. [Crossref] 23. Chandra, S.; Lata, H.; ElSohly, M. A. Em Cannabis sativa L. - Botany and Biotechnology; Chandra, S.; Lata, H.; ElSohly, M. A., eds.; Springer International Publishing: Cham, 2017, p. 84. [Crossref] 24. United Nations Office on Drugs and Crime (UNODC); Recommended Methods for the Identification and Analysis of Cannabis and Cannabis Products, Vienna, 2022. [Link] acessado em setembro 2025 25. Tose, L. V.; Santos, N. A.; Rodrigues, R. R. T.; Murgu, M.; Gomes, A. F.; Vasconcelos, G. A.; Souza, P. C. T.; Vaz, B. G.; Romão, W.; Int. J. Mass Spectrom. 2017, 418, 112. [Crossref] 26. Hall, W.; Addiction 2015, 110, 19. [Crossref] 27. Bechtold, J.; Simpson, T.; White, H. R.; Pardini, D.; Psychology of Addictive Behaviors 2015, 29, 3. [Crossref] 28. Habboushe, J.; Rubin, A.; Liu, H.; Hoffman, R. S.; Basic Clin. Pharmacol. Toxicol. 2018, 122, 660. [Crossref] 29. Holitzki, H.; Dowsett, L. E.; Spackman, E.; Noseworthy, T.; Clement, F.; CMAJ Open 2017, 5, 4. [Crossref] 30. Bachhuber, M.; Arnsten, J. H.; Wurm, G.; J. Psychoact. Drugs 2019, 51, 5. [Crossref] 31. Brown, J. D.; Winterstein, A. G.; J. Clin. Med. 2019, 8, 7. [Crossref] 32. Abrams, D. I.; Eur. J. Intern. Med. 2018, 49, 7. [Crossref] 3. Whiting, P. F.; Wolff, R. F.; Deshpande, S.; Nisio, M. D.; Duffy, S.; Hernandez, A. V.; Keurentjes, J. C.; Lang, S.; Misso, K.; Ryder, S.; Schmidlkofer, S.; Westwood, M.; Kleijnen, J.; JAMA 2015, 313, 24566. [Crossref] 34. Wong, S. S.; Wilens, T. E.; Pediatrics 2017, 140, 5. [Crossref] 35. Hill, K. P.; JAMA 2019, 322, 974. [Crossref] 36. Burggren, A. C.; Shirazi, A.; Ginder, N.; London, E. D.; The American Journal of Drug and Alcohol Abuse 2019, 45, 6. [Crossref] 37. Pisanti, S.; Malfitano, A. M.; Ciaglia, E.; Lamberti, A.; Ranieri, R.; Cuomo, G.; Abate, M.; Faggiana, G.; Proto, M. C.; Fiore, D.; Laezza, C.; Bifulco, M.; Pharmacol. Ther. 2017, 175, 133. [Crossref] 38. Vida Moderna, Mercado de Cannabis Medicinal deve Atingir R$ 1 bi em 2025, https://surl.li/ztxksn, acessado em setembro 2025. 39. Statistica, Total U.S. Cannabidiol (CBD) Product Sales from 2014 to 2022, https://www.statista.com/statistics/760498/total-us-cbd-sales/, acessado em setembro 2025. 40. Kaya Mind, Anuário da Cannabis Medicinal no Brasil 2023, https://kayamind.com/anuario-da-Cannabis-medicinal-no-brasil-2023/, acessado em setembro 2025. 41. Horth, R. Z.; Crouch, B.; Horowitz, B. Z.; Prebish, A.; Slawson, M.; McNair, J.; Elsholz, C.; Gilley, S.; Robertson, J.; Risk, I.; Hill, M.; Fletcher, L.; Hou, W.; Peterson, D.; Adams, K.; Vitek, D.; Nakashima, A.; Dunn, A.; Morb. Mortal. Wkly. Rep. 2018, 67, 20. [Crossref] 42. Nayyar, G. M. L.; Breman, J. G.; Mackey, T. K.; Clark, J. P.; Hajjou, M.; Littrell, M.; Herrington, J. E.; American Society of Tropical Medicine and Hygiene 2019, 100, 5. [Crossref] 43. Monti, M. C.; Zeugin, J.; Koch, K.; Milenkovic, N.; Scheurer, E.; Bender, K. M. C.; Drug Test. Anal. 2022, 14, 6. [Crossref] 44. Barthlott, I.; Scharinger, A.; Golombek, P.; Kuballa, T.; Lachenmeier, D. W.; Toxics 2021, 9, 6. [Crossref] 45. Lachenmeier, D. W.; Habel, S.; Fischer, B.; Herbi, F.; Zerbe, Y.; Bock, V.; de Rezende, T. R.; Walch, S. G.; Sproll, C.; F1000Research 2020, 8, 1394. [Crossref] 46. Citti, C.; Braghiroli, D.; Vandelli, M. A.; Cannazza, G.; J. Pharm. Biomed. Anal. 2018, 147, 565. [Crossref] 47. ANVISA, Anvisa aprova mais três produtos de Cannabis para uso medicinal, https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2022/anvisa-aprova-mais-tres-produtos-de-cannabis-para-uso-medicinal, acessado em setembro 2025. 48. Gov.br, Produtos à Base de Cannabis Poderão ser Regularizados para Uso em Animais, https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2024/produtos-a-base-de-cannabis-poderao-ser-regularizados-para-uso-em-animais, acessado em setembro 2025. 49. Lazarjani, M. P.; Young, O.; Kebede, L.; Seyfoddin, A.; Journal of Cannabis Research 2021, 3, 32. [Crossref] 50. Nahar, L.; Uddin, S. J.; Alam, M. A.; Sarker, S. D.; Phytochem. Anal. 2020, 32, 3. [Crossref] 51. Agarwal, C.; Máthé, K.; Hofmann, T.; Csóka, L.; J. Food Sci. 2018, 83, 3. [Crossref] 52. Rovetto, L. J.; Aieta, N. V.; J. Supercrit. Fluids 2017, 129, 16. [Crossref] 53. Borille, B. T.; González, M.; Steffens, L.; Ortiz, R. S.; Limberger, R. P.; Drug Analytical Research 2017, 1, 1. [Crossref] 54. Lazarjani, M. P.; Torres, S.; Hooker, T.; Fowlie, C.; Young, O.; Seyfoddin, A.; Journal of Cannabis Research 2020, 2, 35. [Crossref] 55. Hall, D. R.; Sinclair, J. S.; Bhuyan, D. J.; Khoo, C.; Li, C. G.; Sarris, J.; Low, M.; Talanta Open 2022, 5, 100112. [Crossref] 56. Dadiotis, E.; Mitsis, V.; Melliou, E.; Magiatis, P.; Molecules 2022, 27, 9. [Crossref] 57. Hazekamp, A.; Choi, Y. H.; Verpoorte, R.; Chem. Pharm. Bull. 2004, 52, 718. [Crossref] 58. Reis, D. S. A.; Rocha, C. M.; Machado, Y.; Fátima, A.; Revista Brasileira de Criminalística 2024, 13, 176. [Crossref] 59. Araneda, J. F.; Chu, T.; Leclerc, M. C.; Riegel, S. D.; Spingarn, N.; Anal. Methods 2020, 12, 4853. [Crossref] 60. Protti, M.; Brighenti, V.; Battaglia, M. R.; Anceschi, L.; Pellati, F.; Mercolini, L.; ACS Med. Chem. Lett. 2019, 10, 4. [Crossref] 61. Hädener, M.; König, S.; Weinmann, W.; Forensic Sci. Int. 2019, 299, 142. [Crossref] 62. Ciolino, L. A.; Ranieri, T. L.; Taylor, A. M.; Forensic Sci. Int. 2018, 289, 438. [Crossref] 63. Brighenti, V.; Pellati, F.; Steinbach, M.; Maran, D.; Benvenuti, S.; J. Pharm. Biomed. Anal. 2017, 143, 228. [Crossref] 64. Swift, W.; Wong, A.; Li, K. M.; Arnold, J. C.; Mcgregor, I. S.; PLoS One 2013, 8, 7. [Crossref] 65. Taschwer, M.; Schmid, M. G.; Forensic Sci. Int. 2015, 254, 167. [Crossref] 66. de Souza, M. R.; Koetz, M.; Limberger, R. P.; Henriques, A. T.; Phytochem. Anal. 2022, 33, 999. [Crossref] 67. Nahar, L.; Onder, A.; Sarker, S. D.; Phytochem. Anal. 2019, 31, 413. [Crossref] 68. Maldaner, L.; Jardim, I. C. S. F.; Scientia Chromatographica 2012, 4, 197. [Crossref] 69. Johnson, E.; Kilgore, M.; Babalonis, S.; Drug Alcohol Depend. 2022, 237, 109522. [Crossref] 70. Huang, S.; Claassen, F. W.; van Beek, T. A.; Chen, B.; Zeng, J.; Zuilhof, H.; Salentijn, G. I. J.; Anal. Chem. 2021, 93, 3794. [Crossref] 71. Manca, A.; Palermiti, A.; Mula, J.; De Vivo, E. D.; Zeaiter, S.; Simiele, M.; De Nicolò, A.; Cantù, M.; Cusato, J.; D'Avolio, A.; Phytomedicine 2022, 102, 154218. [Crossref] 72. Morini, L.; Porro, G.; Liso, M.; Groppi, A.; Curr. Pharm. Biotechnol. 2018, 18, 828. [Crossref] 73. Calvi, L.; Pentimalli, D.; Panseri, S.; Giupponi, L.; Gelmini, F.; Beretta, G.; Vitali, D.; Bruno, M.; Zilio, E.; Pavlovic, R.; Giorgi, A.; J. Pharm. Biomed. Anal. 2018, 150, 208. [Crossref] 74. Agência Nacional de Vigilância Sanitária (Anvisa); Resolução da Diretoria Colegiada (RDC) No. 166, de 24 de julho de 2017, Dispõe sobre a Validação de Métodos Analíticos e dá Outras Providências; Diário Oficial da União (DOU), Brasília, Brasil, 2017. [Link] acessado em setembro 2025 75. DOQ-CGCRE-008: Orientação sobre Validação de Métodos Analíticos; INMETRO: Rio de Janeiro, 2020. [Link] acessado em setembro 2025 76. Demartini, D. R.; Tandem Mass Spectrometry - Molecular Characterization; Coelho, A. V.; Franco, C. M. F., eds.; Intechopen: London, 2013. [Crossref] 77. Peters, F. T.; Drummer, O. H.; Musshoff, F.; Forensic Sci. Int. 2007, 165, 216. [Crossref] 78. European Medicines Agency; ICH Q2(R2) - Guideline on Validation of Analytical Procedures, 2024. [Link] acessado em setembro 2025 79. Uhrovčík, J.; Talanta 2014, 119, 178. [Crossref] 80. McEnroe, R. J.; Durham, A. P.; Goldford, M. D.; Kondratovich, M. V.; Lababidi, S.; Magari, R.; Middle, J. G.; Pierson-Perry, J. F.; Vaks, J. E.; Evaluation of Precision of Quantitative Measurement Procedures, 3rd ed.; Clinical and Laboratory Standards Institute: Pennsylvania, 2014. 81. Carvalho, V. M.; Almeida, F. G. D.; Aguiar, A. F. L. D.; Pereira, F. C. D. S.; Rocha, E. D.; Brazilian Journal of Analytical Chemistry 2022, 9, 162. [Crossref] 82. Hsu Y. H.; Fang, M. C.; Huang, S. C.; Kao, Y. M.; Tseng, S. H.; Wang, D. Y.; J. Food Drug Anal. 2021, 29, 502. [Crossref] 83. Palermitti A.; Cafaro, A.; Barco, S.; Bucchioni, P.; Franceschini, P.; Cusato, J.; Nicolò, A. D.; Manca, A.; Vivo, E. D. D.; Russo, E.; Cecchi, F.; Pigliasco, F.; Lillo, F.; Tripodi G.; D'Avolio, A.; Cangemi, G.; Pharmaceuticals 2021, 14, 462. [Crossref] 84. Madej, K.; Kózka, G.; Winiarski, M.; Piekoszewski, W.; Separations 2020, 7, 60. [Crossref] 85. Mandrioli, M.; Tura, M.; Scotti, S.; Toschi, T. G.; Molecules 2019, 24, 2113. [Crossref] 86. Galettis, P.; Williams, M.; Gordon R.; Martin, J. H.; Aust. J. Chem. 2021, 74, 453. [Crossref] |
On-line version ISSN 1678-7064 Printed version ISSN 0100-4042
Qu�mica Nova
Publica��es da Sociedade Brasileira de Qu�mica
Caixa Postal: 26037
05513-970 S�o Paulo - SP
Tel/Fax: +55.11.3032.2299/+55.11.3814.3602
Free access